
产品货号:
JN5112
中文名称:
一步法多片段DNA定向无缝克隆试剂盒
英文名称:
BalbRec plus One step PCR Cloning Kit
产品规格:
20T|40T
发货周期:
1~3天
产品价格:
询价

本试剂盒是一款简便、快速、高效的多片段DNA定向无缝克隆产品,可以不受载体和目的片段的酶切位点限制,直接用同源重组的方法将PCR产物定向克隆至任意载体的任意位点,完成目的片段与载体相连接的基因克隆技术。在克隆前,需要先将载体线性化,并在插入片段正、反向PCR引物5'端引入15~25bp的线性化载体末端同源序列,使得PCR产物5'和3'末端分别带有与线性化载体两末端对应的完全一致的同源序列。插入片段和线性化载体以一定比例混合,在重组酶的作用下,最快仅需50℃反应5min即可进行重组连接,完成定向克隆,克隆阳性率可达95%以上。
本试剂盒采用最新优化工艺,可以高效兼容1-12个DNA片段的同源重组,并且进一步提升了对DNA投入量的兼容性,极大地减轻了由于DNA片段浓度低导致克隆效率下降的困扰。

- 高效:一步定向克隆1~12片段,无缝拼接;
- 快速:2片段以内连接仅需5min;
- 兼容:低投入量片段连接效率高;
- 齐全:试剂盒提供菌落鉴定PCR Mix。

快速克隆、高通量克隆、DNA定点突变。

| 组分 | 20T | 40T |
| 2×BalbRec Plus Recombinase Mix | 200μL | 200μL×2 |
| BalbRec pUC19(线性,50ng/μL) | 10μL | 10μL |
| 800bp PCR片段(阳性对照,50ng/μL) | 10μL | 10μL |
| 2×Complex Taq MasterMix | 1mL | 1mL×2 |
保存:-20℃,避免反复冻融,有效期1年。

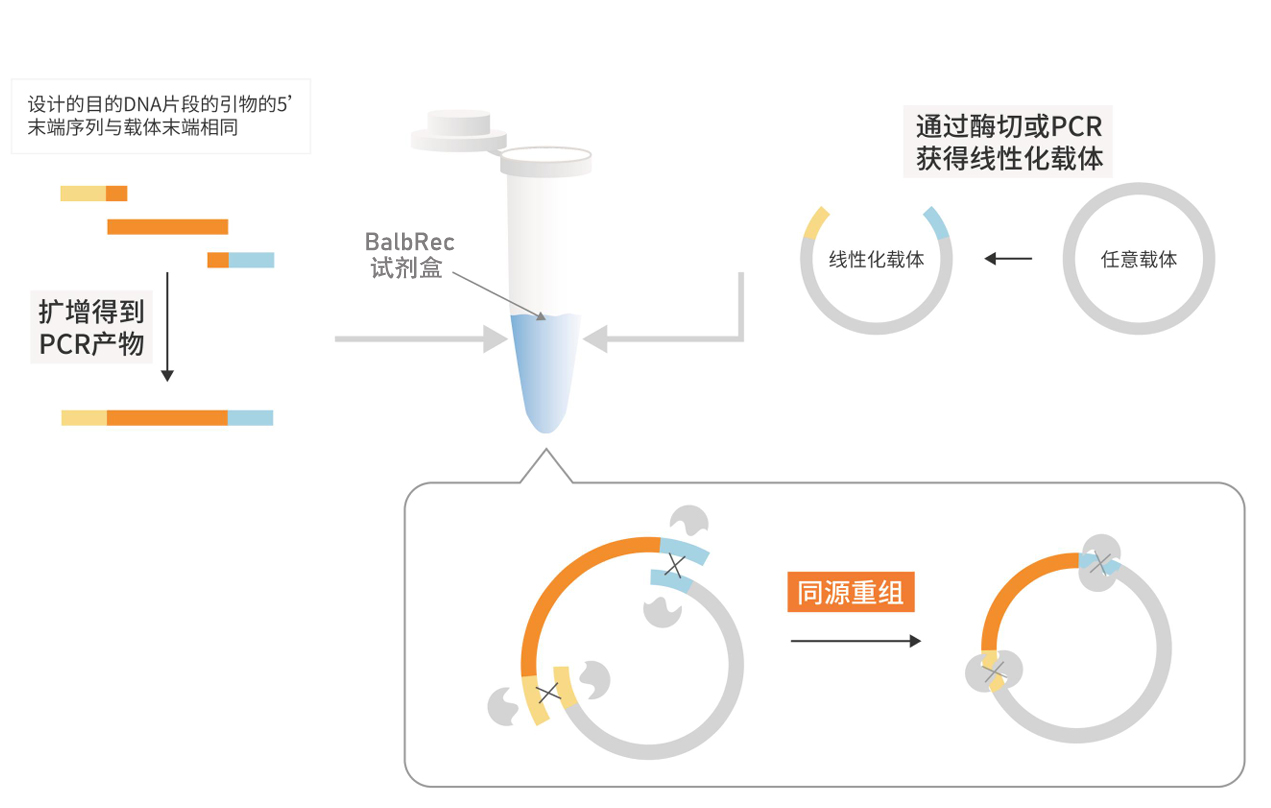

- 载体制备
选取合适的位点,单酶切,双酶切或PCR扩增皆可,并且5'端粘性末端、3'端粘性末端或平末端均适用本试剂盒。由于单酶切线性化程度差,且为了提高阳性率,载体线性化方式建议采取双酶切或反向PCR扩增。最终载体的浓度>15ng/μL(高浓度的载体有利于提高克隆效率)。 - 引物设计与目的片段的获得
使用一步定向克隆试剂盒时,引物设计非常重要,总原则是通过引物在目的片段的上下游分别引入15~25bp的同源重组序列,各目的片段与线性化克隆载体之间能够同源互补序列进行克隆连接。即在遵循引物设计基本原则的前提下,只需要在目的片段上下游引物的5’端加上15~25bp与载体或相邻片段同源的序列。
目的片段通常通过PCR获得,为保证PCR扩增的特异性及灵敏度,请尽可能选用高保真酶,推荐使用2×Fast Pfu MasterMix。引物设计长度至少在30~50bp,包括15~25bp 5'端与载体同源的序列和15~25bp目的片段特异性序列。- 如果是表达载体克隆构建,引物设计完成后,请注意检查开放阅读框是否正确;
- PCR扩增结束后如有杂带,需切胶回收,否则杂带会影响重组反应。
- 单片段同源重组引物设计的总原则:
在插入片段的正反向扩增引物的5'端引入线性化载体两末端的同源序列,使得到的插入片段5'和3'末端分别带有和线性化克隆载体两末端对应的同源序列(15~25bp,不包括酶切位)。
插入片段正向扩增引物设计方式为:
5'-上游载体末端同源序列+酶切位点(可保留或删除)+正向扩增引物序列-3'
插入片段反向扩增引物设计方式为:
5'-下游载体末端同源序列+酶切位点(可保留或删除)+反向扩增引物序列-3'
可参照以下单片段连接引物设计案例: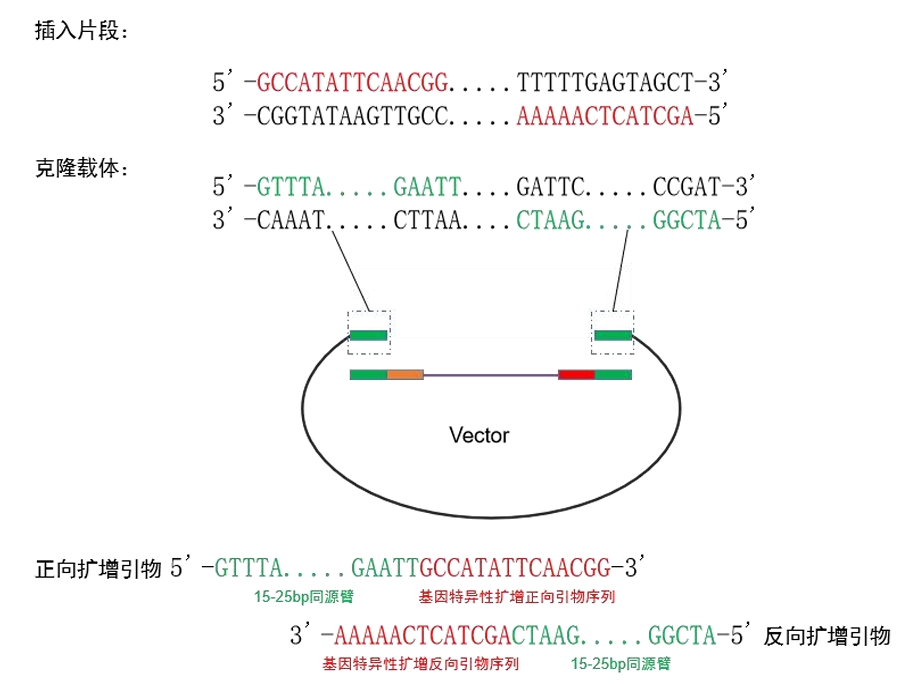
图2.单片段扩增引物设计方案- 若最终引物长度超过40bp,推荐在引物合成时选用PAGE纯化,可提高克隆成功率。
- 多片段同源重组引物设计的总原则:
通过在引物5'端引入同源序列,使扩增产物之间以及扩增产物与线性化克隆载体之间都具有能够相互同源重组的序列(15~25bp),不包括酶切位点。
两侧片段与载体重组端的引物设计方式为:
最上游片段正向扩增引物:
5'-上游载体末端同源序列+酶切位点(可保留或删除) +正向扩增引物序列-3'
最下游片段反向扩增引物:
5'-下游载体末端同源序列+酶切位点(可保留或删除) +反向扩增引物序列-3'
中间各插入片段扩增引物设计方式为:
用于片段之间进行重组的同源序列可以添加至前方片段的反向扩增引物中,也可以添加至后方片段的正向扩增引物中,还可以两片段各添加一部分。- 正/反向扩增引物序列即常规插入片段正/反向扩增引物序列,Tm值60~65℃为佳;
- 上/下游载体末端同源序列即线性化载体最末端序列(用于同源重组),GC含量40%~60%为佳。
图3.多片段扩增引物设计方案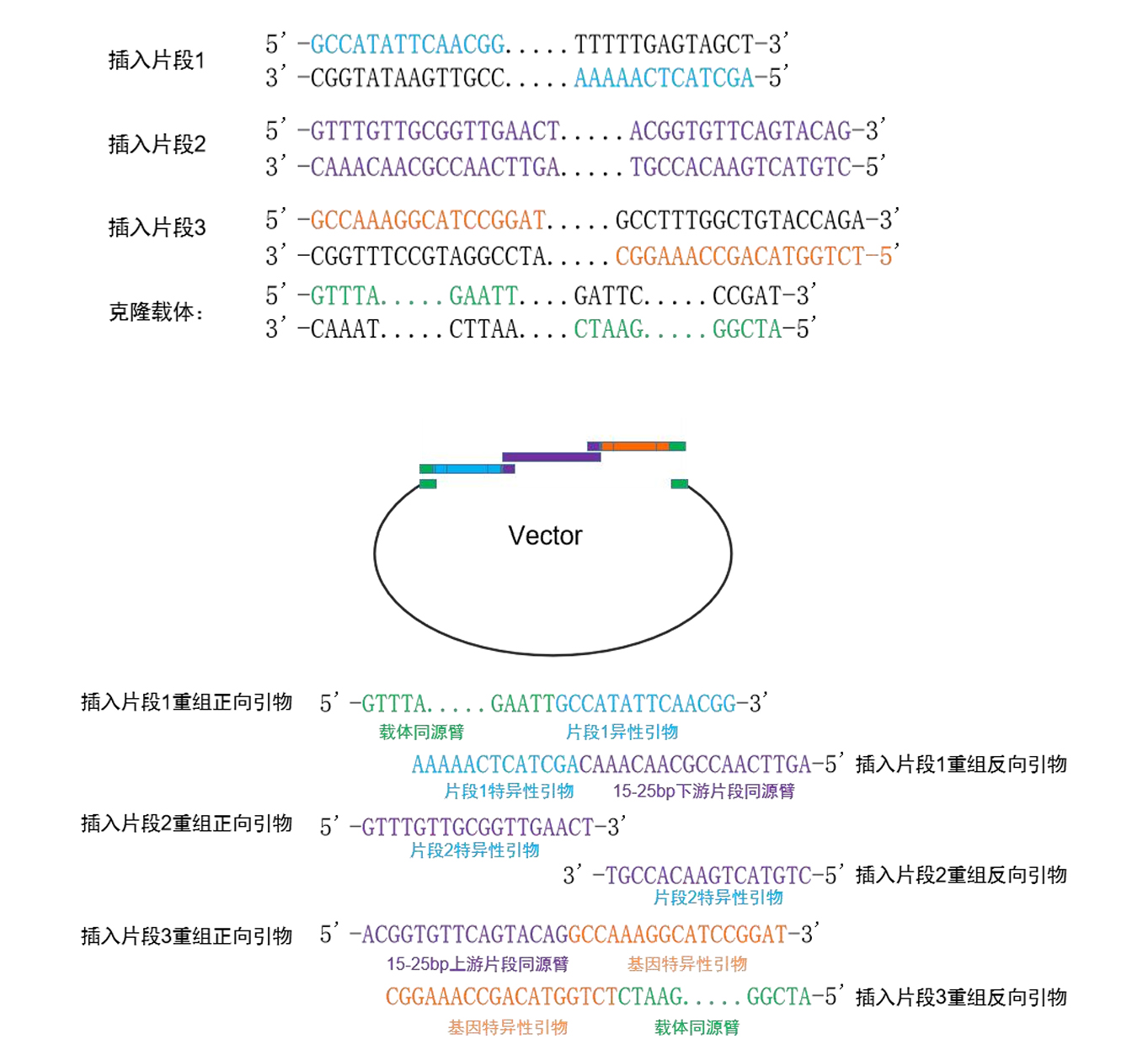
- 正/反向扩增引物序列即常规插入片段正/反向扩增引物序列,Tm值60~65℃为佳;
- 如果是表达载体克隆构建,引物设计完成后,请注意检查开放阅读框是否正确;
- 目的基因与载体重组
- 于冰盒上将线性化载体与目的片段以一定的摩尔比加入到离心管中进行重组反应,反应体系见下表。
试剂 1~2片段连接 3片段连接 4~12片段连接 阳性对照 载体加量 X μL X μL X μL 1μL 插入片段加量 Y μL Y μL Y μL 1μL 载体与插入片段的摩尔比 1∶2 1∶2 1∶1 1∶2 2×BalbRec Plus Recombinase Mix 10μL RNase Free Water 至20μL 反应时间 50℃,5min 50℃,10min 50℃,30~40min 50℃,5min - 当载体加入量为100~200ng时,可获得较高的重组效率。
- 本制品可兼容0.003pmol的载体与片段的投入量,所以当载体和插入片段总体积>10μL时,可适当降低投入量,但注意反应时间不要超过推荐时间。
- 4~12片段连接建议各片段的引物同源臂长度大于20bp,各片段与载体的摩尔比分别为1:1,反应时间可延长到30~40min,最长不要超过1h。
- 阳性对照用试剂盒提供的BalbRecpUC19(Linearized,50ng/μl)线性化载体,插入片段用试剂盒提供的800bp PCR Fragments (Positive Control,50ng/μL)片段。
- 对于单片段同源重组反应:
最适克隆载体使用量=(0.02×克隆载体碱基对数)ng,换算为摩尔质量=0.03pmol;
最适插入片段使用量=(0.04×插入片段碱基对数)ng,换算为摩尔质量=0.06pmol。 - 对于多片段同源重组反应:
最适克隆载体使用量=(0.02×克隆载体碱基对数)ng,换算为摩尔质量=0.03pmol;
每个片段的最适使用量=(0.02×每个片段碱基对数)ng,换算为摩尔质量=0.03pmol。
- 当载体加入量为100~200ng时,可获得较高的重组效率。
- 反应结束可直接进行转化,若不转化需储存在4℃或-20℃。
- 于冰盒上将线性化载体与目的片段以一定的摩尔比加入到离心管中进行重组反应,反应体系见下表。
- 反应产物转化、涂板
建议所使用的感受态细胞效率≥1×108cfu/μg。转化步骤如下:- 冰上融化一管100μL的DH5α感受态细胞,轻弹管壁使细胞重悬起来。加入10μL的反应液到感受态细胞中,轻弹数下,冰浴30min;
- 42℃水浴中热激90sec后快速放入冰上5min;
- 加入900μlSOC或LB液体培养基,37℃孵育45~60min;
- 5000rpm离心3分钟收集菌体,根据需要将一定量的菌体均匀的涂布在含抗生素平板上。
- 具体操作请参考对应感受态操作说明书,如菌落数过多可以适当减少涂板量。
- 为了验证载体酶切完全,建议做转化的同时做一个空载体作为对照。在载体处理好的情况下,对照应无克隆生长!
- 具体操作请参考对应感受态操作说明书,如菌落数过多可以适当减少涂板量。
- 冰上融化一管100μL的DH5α感受态细胞,轻弹管壁使细胞重悬起来。加入10μL的反应液到感受态细胞中,轻弹数下,冰浴30min;
- 阳性克隆鉴定
一般建议采用菌落PCR进行阳性克隆鉴定。试剂盒内配套提供2×Complex Taq MasterMix(可用于阳性克隆鉴定。- 鉴定引物的选择:为了避免假阳性结果,我们建议一条引物为载体特异性引物,另一条引物为目的片段特异性引物。

- 引物如何设计?
在选择克隆位点时,应选择ATCG分布较为均匀的区域设计引物。并且当同源臂的GC含量均在40%~60%范围内时,重组效率将达到最大,当引物长度>40bp时,在引物合成时建议使用PAGE纯化。 - 重组构建
- 目的片段与载体摩尔比的计算
若是1~3片段相连接,载体与插入片段的摩尔比为1:2,若是4~6片段相连接,载体与插入片段的摩尔比为1:1,从而保证所有片段与载体的摩尔比是一样的。 - 目的片段或载体过大,怎么处理?
在设计引物时,将与载体同源的序列由常规的15~20bp大小增加至20~40bp;
载体或目的片段过大(大于8kb),需要增加反应中载体总量,建议一次反应至少加入100ng载体。
选用转化效率高的感受态细胞。 - 单酶切(黏性末端,平末端)处理的载体片段,是否影响阳性率?
实验证明,单酶切或双酶切获得的线性化载体,无论是粘性末端还是平末端,他们在重组反应中的效率是一样的,需要提醒的是,载体酶切一定要完全,否则未切开的载体会影响后续的阳性克隆鉴定。
- 目的片段与载体摩尔比的计算
- Taq DNA聚合酶扩增后末端加A影响重组效率吗?
目的片段用Taq DNA聚合酶扩增后是3’端增加A,不会影响重组效率。 - 同源序列不完全匹配会不会影响重组效率?
同源序列不完全匹配,则会影响重组效率的。所以除非是特殊原因,否则在设计时,同源序列最好是相匹配的。 - 转化后未长出菌落或菌落数少,是什么原因?
首先使用阳性对照,可排除试剂盒本身的影响。- 转化的平板无克隆生长,如果阳性对照也无克隆生长,可能原因是:
- 平板的抗性错误或放置时间过长,建议重新转化,在抗性正确、新鲜配置的平板上进行培养;
- 感受态细胞转化效率太低,建议使用高效的感受态细胞,确保转化效率≥108cfu/μg;可以对感受态转化效率进行检测,转化0.1ng质粒,取1/10进行涂板,生长菌落数≥1000,估算转化效率为108cfu/μg;重组产物的转化体积不应超过感受态细胞体积的1/10,否则会降低转化效率;选择克隆用感受态细胞(如DH5α),不能选择表达感受态细胞;
- 试剂盒保存不当,酶失活了,建议使用新的试剂盒。
- 平板的抗性错误或放置时间过长,建议重新转化,在抗性正确、新鲜配置的平板上进行培养;
- 转化的平板不长,但是阳性对照长了,可能原因是:
- 同源序列过短,导致同源重组不能有效的进行,建议增加目的片段与载体的同源序列,应保证同源序列的长度达到15~20bp;
- 培养条件有误,应注意培养箱的培养温度是否适宜,培养时间是否足够;
- 如果克隆基因表达产物对宿主有毒性,需选择极低表达背景的启动子和使用低拷贝克隆载体;
- 感受态细胞转化效率太低,建议使用高效的感受态细胞,确保转化效率≥108cfu/μg;
- 目的片段引物设计不正确。引物设计应包含15~25bp的同源臂,同源臂的GC含量在40%~60%之间为佳;
- 载体和插入片段上样量不足或者载体/片段摩尔比未达到1:2或1:1;
- 载体、片段未纯化或纯化效率低,建议使用纯化后的载体和片段进行克隆,纯化后需用Nanodrop测试纯度。
- 同源序列过短,导致同源重组不能有效的进行,建议增加目的片段与载体的同源序列,应保证同源序列的长度达到15~20bp;
- 转化的平板无克隆生长,如果阳性对照也无克隆生长,可能原因是:
- 转化后克隆在板上长得很好,就是没有阳性,是什么原因?
- 载体线性化不完全,载体酶切时,加入量太多,或酶切时间太短,导致载体未完全线性化,建议重新处理载体;推荐进行线性化载体转感受态测试,如未长菌落即可确认线性化完全;
- LB平板存放时间太长了,抗性减少或消失,建议重新配制新鲜的LB平板;
- 确定阳性鉴定的方法(引物、PCR条件)是否有问题,是否会漏检出阳性克隆;
- 反应体系被其他具有相同抗性的质粒污染,应确保在转化的过程中无其他杂菌污染;
- 菌落PCR扩增引物不正确,推荐使用一条载体上的通用引物和一条目的片段的特异性引物进行菌落PCR;
- PCR体系或反应程序不合适:没有目的条带也没有空质粒条带,建议更换更合适的PCR体系、反应程序(尤其是Tm温度);或者提取质粒,以质粒做模板PCR验证;或者进行酶切验证。
- 载体线性化不完全,载体酶切时,加入量太多,或酶切时间太短,导致载体未完全线性化,建议重新处理载体;推荐进行线性化载体转感受态测试,如未长菌落即可确认线性化完全;
- 鉴定有阳性,但是测序不是目的基因,为什么?
- 引物特异性不强,扩增到的不是目的基因,建议重新设计引物进行PCR扩增;
- 模板上无目的基因,建议将模板测序,确定模板的正确性;
- 反应体系被污染,建议目的基因扩增后割胶回收;
- 鉴定阳性克隆的引物设计有误,推荐使用一条载体上的通用引物和一条目的片段的特异性引物进行测序。
- 引物特异性不强,扩增到的不是目的基因,建议重新设计引物进行PCR扩增;
- 阳性克隆测序后发现在序列的引物处有碱基突变,是什么原因引起的?
- 引物合成有错误,建议采用高纯度的引物;
- 目的片段切胶回收时,在紫外灯下不能暴露过长时间,UV照射会引起较高的突变;
- 目的片段扩增时DNA聚合酶保真度不高导致碱基突变,建议使用高保真度的DNA聚合酶。
- 引物合成有错误,建议采用高纯度的引物;
相关搜索:一步法多片段DNA定向无缝克隆试剂盒,无缝克隆,BalbRec plus One step PCR Cloning Kit



